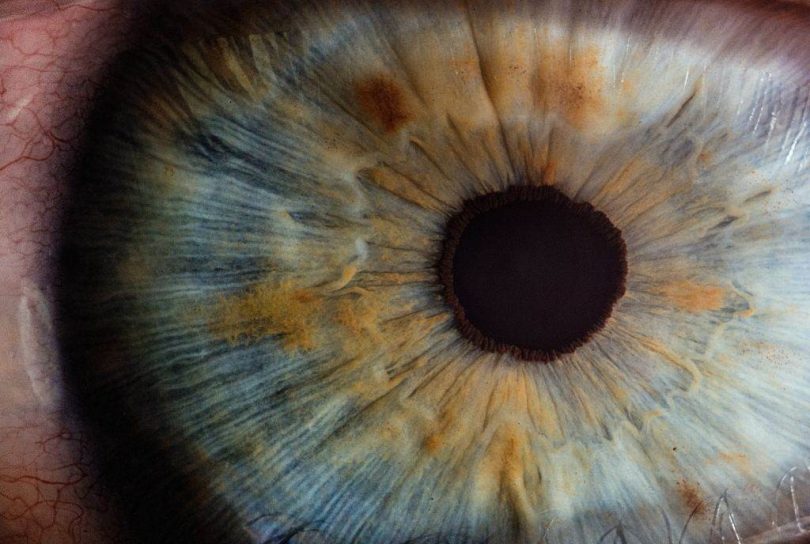
У међувремену очи донора и животињски модели ће морати да одрађују посао, а тестирање на b-таласе могло би бити добар начин да се утврди да ли је трансплатација жуте мрље одржива или не.
Најновија студија је потврдила да је могуће вратити активност ћелија у људском оку на неколико сати после смрти – наговештавајући да ћемо ускоро моћи да се изборимо са неповратном природом смрти централног нервног система. Да би боље разумели начин на који нервне ћелије реагују на недостатак кисеоника, тим америчких истраживача је измерио активност у ћелијама мрежњаче код миша и код човека убрзо након њихове смрти.
Ово је први пут да су очи умрлих донора – људи – икада реаговале на светлост на овај начин, а неки стручњаци доводе у питање „неповратну природу” смрти централног нервног система.
Стимулисане светлошћу, показало се да post mortem мрежњаче емитује специфичне електричне сигнале, познате као b-таласи. На овај начин ћелије су успеле да комуницирају и до неколико сати након смрти. Ово је први пут да су очи умрлих донора – људи – икада реаговале на светлост на овај начин, а неки стручњаци доводе у питање „неповратну природу” смрти централног нервног система.
„Успели смо да пробудимо фоторецепторске ћелије у жутој мрљи, која је део мрежњаче и одговорна је за централни вид и способност људи да виде фине детаље и боју”, објашњава биомедицинска научница Фатима Абас са Универзитета Јута. „Ћелије у очима које су добијене пет сати након смрти донора, реаговале су на јако светло, обојена светла, па чак и на веома слабе бљескове светлости.”
Нова сазнања о томе како се одабрана ткива у нервном систему носе са губитком кисеоника могло би да нас науче новим стварима о опоравку изгубљених можданих функција.
Kако функционише наше тело након смрти? Поједине органе је могуће сачувати за трансплантацију непосредно након смрти. Али када циркулација стане, централни нервни систем у целини престаје да реагује, а органи престају да буду одговарајући за било који облик дугорочног опоравка. Ипак, не пропадају сви типови неурона истом брзином. Различити региони и различите врсте ћелија имају различите механизме преживљавања, што питање смрти мозга чини много компликованијим.
Нова сазнања о томе како се одабрана ткива у нервном систему носе са губитком кисеоника могло би да нас науче новим стварима о опоравку изгубљених можданих функција. Научници са Универзитета Јејл су 2018. године доспели на насловне стране када су одржавали свињски мозак у животу чак 36 сати након смрти. То су постигли заустављањем брзе деградације неурона, коришц́ењем вештачке крви, грејача и пумпи за обнављање циркулације кисеоника и хранљивих материја.
Враћањем кисеоника и неких хранљивих материја у очи донатора органа, истраживачи са Универзитета Јута успели су да покрену синхрону активност међу неуронима након смрти. „Успели смо да натерамо ц́елије мрежњаче да комуницирају једна са другом, на начин на који то раде у оку живог човека”, каже научник Франс Винберг са Универзитета Јута.
Експерименти су показали да ћелије мрежњаче у почетку настављају да реагују на светлост. То траје до пет сати након смрти. Ипак, кључни међућелијски сигнали b-таласа брзо су нестали, очигледно због губитка кисеоника. Чак и онда када је ткиво мрежњаче било пажљиво заштићено од недостатка кисеоника, истраживачи нису успели у потпуности да обнове ове b-таласе.
Ако специјализовани неурони, познати као фоторецептори, могу да се оживе до одређене мере, онда то буди наду за будуће трансплантације које би могле помоћи у обнављању вида људи са очним болестима.
Да ли можемо да победимо мождану смрт? Према неким дефиницијама „мождана смрт” је губитак синхроне активности међу неуронима. Ако прихватимо овакву дефиницију, онда људске мрежњаче нису биле потпуно мртве. „Пошто је ретина део централног нервног система, рестаурација б-таласа у овој студији поставља питање да ли је мождана смрт, заиста неповратна”, пишу аутори.
Ако специјализовани неурони, познати као фоторецептори, могу да се оживе до одређене мере, онда то буди наду за будуће трансплантације које би могле помоћи у обнављању вида код људи са очним болестима. Тај дан је, тврде научници, ипак још далеко. Трансплатација ћелија и делова мрежњаче донатора би морали некако да буду неприметно интегрисани у постојеће ретиналне кругове, што је изазов с којим научници већ покушавају да се позабаве.
У међувремену очи донора и животињски модели ће морати да одрађују посао, а тестирање на b-таласе могло би бити добар начин да се утврди да ли је трансплатација жуте мрље одржива или не. Студија је објављена у часопису Nature.
(Извор Национална географија)